الإنثالبي (المحتوى الحراري) Enthalpy
- یعبر الكیمیائیون عن كمیة الحرارة التي تمتص أو تنبعث بواسطة عملیات عند الضغط الثابت بالأنثالبي (H) حیث أن أنثالبي التفاعل یساوي الفرق بین الأنثالبي للنواتج والأنثالبي للمتفاعلات.
- الإنثالبي ، أو المحتوى الحراري ھو "الطاقة المختزنة في مول من المادة"
- يرمز للمحتوى الحراري بالرمز (H) وھو خاصیة ممیزة للمادة (تماماً كالكتلة والحجم)، فكل مادة لھا كمیة محددة من الإنثالبي.
حرارة التفاعل Heat of Reaction
- يمكن تعريف حرارة التفاعل بأكثر من طريقة :
(1) حرارة التفاعل: ھي محصلة تغیرات الطاقة الناتجة عن تحطیم وتكوین الروابط الكیمیائیة.
(2) حرارة التفاعل: هي كمیة الحرارة التي تنطلق أو تمتص عندما یتفاعل عدد من الجزیئات مع بعضھا لینتھي التفاعل بالنواتج.
(3) حرارة التفاعل : هي الفرق بین حرارة المواد المتفاعلة (ΔHReactants) حرارة المواد الناتجة (ΔHProducts)".
وقد یكون ھذا التغیر الحراري مصاحباً لعملیة تكوین مادة من عناصرھا الأولیة، وفي ھذه الحالة یسمى ذلك التغیر الحراري "حرارة التكوین". أو یكون ھذا التغیر الحراري مصاحباً لعملیة احتراق مادة ما فیسمى "حرارة الإحتراق"، أو یكون مصاحباً لعملیة تعادل بین حمض وقاعدة، فیسمى " حرارة التعادل"، ... وھكذا.
حساب قيمة الإنثالبي ΔH للتفاعلات
- یمكن حساب التغیر في الإنثالبي ΔH للتفاعل بطرح انثالبي المواد المتفاعلة من انثالبي المواد الناتجة.
حيث :
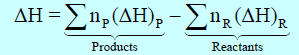
P تعني Products أي النواتج ، R تعني Reactants أي المتفاعلات .
np= عدد مولات المواد الناتجة ، nR = عدد مولات المواد المتفاعلة.
ΔH)p) = انثالبي النواتج ، ΔH)R) = انثالبي المتفاعلات
- وعند كتابة قیمة الإنثالبي في المعادلة فإنھا تعرف بالمعادلة الكیمیائیة الحراریة (thermochemical equation) كما في المثالین التالیین :
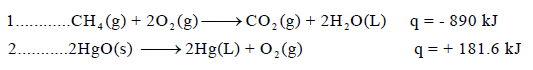
في التفاعل الأول قیمة التغیر في الإنثالبي بالسالب (ΔH = - 890kJ) وبالتالي فإن التفاعل طارد للحرارة، وفیه یكون انثالبي المواد الناتجة أقل من انثالبي المواد المتفاعلة وفقاً للعلاقة:
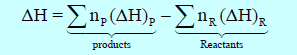
وفي التفاعل الثاني فإن قیمة التغیر في الإنثالبي (حرارة التفاعل) موجبة ( (ΔH = + 181.6 kJ وبالتالي فإن التفاعل یكون ماصاً للحرارة، وحینھا فإن انثالبي المواد المتفاعلة وفقاً للعلاقة:
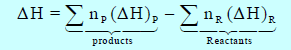
موضوعات هامة لحساب الأنثالبي
- يمكنك حساب الأنثالبي لكل نوع من أنواع الأنثالبي من خلال قراءة وتصفح الروابط الآتية:
(1) حرارة التكوين Heat of Formation + مسائل محلولة
(2) حرارة الإحتراق وحرارة التعادل Heat of Combustion and Heat of Neutralization
(3) حرارة الإذابة Heat of solution
(4) أنواع حرارات التفاعل Types of Heat (enthalpy) of Reaction
كما يمكنك قراءة هذة الموضوعات الرائعة أيضاً لحساب الإنثالبي:
(5) حساب الأنثالبي عن طريق قانون هس Hess law + مسائل محلولة
(6) مسائل محلولة على الكيمياء الحرارية
(7) مسائل محلولة على العلاقة بين الأنتروبي والإنثالبي وطاقة جبس الحرة