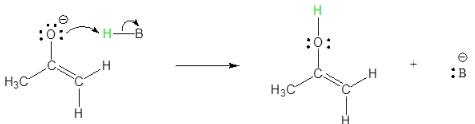التشكل التوتوميري Tautomerism
- هي أزواج من ايزوميرات الشكل أو الهيكل (المماكبات أو المصاوغات أو المتشابهات الصيغ) يمكن ان تتبادل فيما بينها بواسطة تفاعل كيميائي متعاكس .هذه العملية أو التفاعل يسمى تاوتمرة Tautomerism.
- في هذا التفاعل تنزاح ذرة من الهيدروجين مع تغيير مكان الرابطة المزدوجة.
- تشكل يحدث في المركبات التي تحتوي علي ذرة هيدروجين فى الوضع ألفا (مجاور) بالنسبة لمجموعة كربونيل.
- هذه المركبات يمكن أن توجد في حالة توازن بين صيغتين اخداهما تسمي (كيتو) والاخري تسمي (اينول) وتعرف هاتان الصيغتان باسم المتشكلات التوتوميرية ويقصد به:
وجود صيغتين لمركب واحد يختلفان فقط في مكان بروتون واحد حيث يكون هذا البروتون في احدي الصيغتين متصلا بذرة كربون (الكيتو) وفي الصيغة الثانية (الاينول) بذرة اكسيجين.
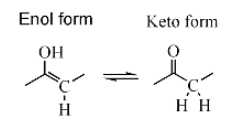
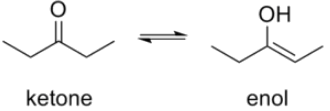
- إنّ اكثر أنواع التوتوميرية شيوعيا تلك الأنواع التي يدخل فيها مركبات الكربونيل أو الكيتو و مركبات الهيدروكسيل غير المشبعة، أو الإينولات؛ و يحدث التغير في التركيب البنائي عن طريق تحريك ذرّة الهيدروجين بين ذرّات الكربون و الأوكسجين , مع إعادة تنظيم للروابط.
- في العديد من المركبات الألدهيدية أو الكيتونية الاليفاتية ، مثل الأسيتالديهايد، فإن شكل الكيتو هو السائد؛ أما في الفينولات، فإن شكل الإينول هو السائد . و هناك حالة وسط تتمثل في أسيتو خلات الإيثيل ، حيث في درجة حرارة الغرفة يتكون من 92.4 % كيتو و 7.6 % إينول .
- بالأضافة إلى توتوميرية الإينول -كيتون ، فإنه هناك عدة أنواع أخرى مشهورة، ببما في ذلك مركبات نيترو الأليفاتية و تلك التي تتضمن تراكيب السلاسل و الحلقات و خصوصا من جزيئات السكّريات.
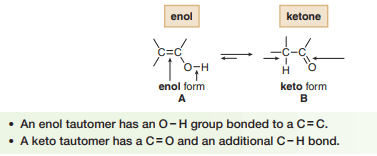
صيغة الأينول - كيتو للأسيتون Enol - keto forms in Acetone
- حالة الأتزان بين الاينول - كيتو تكون بطيئة فى الظروف العادية.
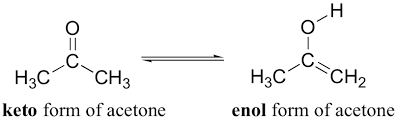
- الأكثر ثباتاً هنا هو صيغة الكيتو حيث يتواجد بنسبة 99.99% فى الأسيتون.
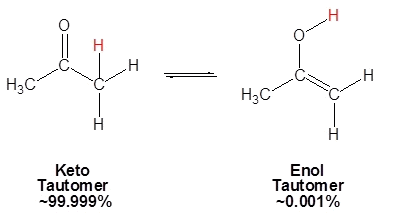
- يتم تحفيز الاتزان بين الاينول - كيتون فى الاسيتون بواسطة كمية قليلة من الأحماض أو القواعد.
أولاً: فى حالة أضافة الأحماض
Protonation of the Carbonyl
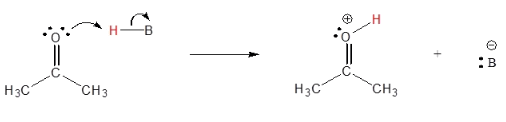
Enol formation
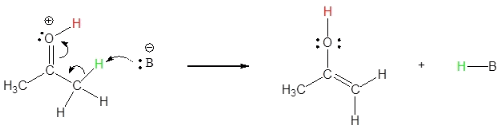
ثانياً: فى حالة إضافة القواعد
Enolate formation
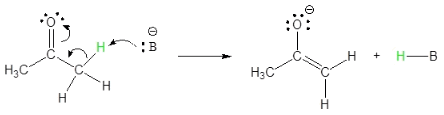
Protonation