كشفت مصادر مطلعة أن الانفجار الذي هز بيروت يوم الثلاثاء 4/8/2020 ناجم عن انفجار مستودع يحتوي على 2700 طن من نترات الأمونيوم، التي تستخدم سماداً زراعياً.
- فى البداية يجب أن نلفت الانتباه أنه يوجد ثلاث أنواع من نترات الأمونيوم المستخدمة فى النقل وهي:
(1) نترات أمونيوم مادة متفجرة رقم الأمم المتحدة له : Un 0222 يحتوى على نسبة أكبر من 0.2 من المواد القابلة للأشتعال.
(2) نترات الأمونيوم سائل مركز ساخن Un 2426
(2) نترات الأمونيوم مادة صلبة رقم الأمم المتحدة له : Un 1942 يحتوى على نسبة أقل من 0.2 من المواد القابلة للأشتعال.
وهنا النوع الثالث هو المتسبب فى انفجار بيروت حسب ما جاء بالأخبار لذلك سوف نستعرض المعلومات الخاصة بالنوع الثالث
الصفات الهامة لنترات الأمونيوم
- هي مركب كيميائي له الصيغة الكيميائية NH4NO3 وهي مادة صلبة بلورية بيضاء سريعة الذوبان فى الماء.
- عامل مؤكسد قوي جداً
- لا يشتعل ولكن يساعد على الاشتعال مع حدوث انفجار عند التسخين أو في حالة وجود مواد أو غازات أو أبخرة مشتعلة بالقرب منه.
- يتفاعل مع المواد القابلة للاشتعال والعوامل المختزلة القوية وسبائك النحاس والمعادن الثقيلة مثل الحديد والقلويات
الخواص الانفجارية لنترات الأمونيوم
- نترات الأمونيوم ليست متفجرة بالشكل الذي تباع فيه عادة ، ولكنها تحت ظروف معينة تكون مدمرة.
- تشكل نترات الأمونيوم بسهولة مخاليط متفجرة بخصائص متفاوتة عند دمجها مع المتفجرات الأولية مثل الأزيدات أو مع الوقود مثل مسحوق الألومنيوم أو زيت الوقود fuel oil
- هناك مجموعة من العوامل والظروف التي لا بد من توافرها لتحويل نترات الأمونيوم من مركب آمن إلى مادة متفجرة، من دون أي وقود أو محفزات خارجية.
- يتم تصنيف نترات الأمونيوم على أنها مادة حيوية ، وهي تنتج الحرارة أثناء تحللها على غرار الطرق المعروفة عن توليد الحرارة باستخدام المواد المتعفنة في السماد.
- إذا كانت هناك كمية كبيرة من نترات الأمونيوم في ظروف غير طبيعية، فإنه يمكنها توليد حرارة ذاتية كافية لإشعال النار واستمرار الحريق، من دون الحاجة إلى أي محفز خارجي.
- أثناء احتراقها، تمر نترات الأمونيوم بتغيرات كيميائية تؤدي إلى إنتاج الأكسجين، وهو بالضبط ما يحتاجه أي حريق للاستمرار والتمدد، ومع ارتفاع درجة الحرارة تتحول المادة إلى ما يشبه "مفجر القنبلة".
خطورة نترات الأمونيوم
- يؤدي إلى تهيج شديد وإحمرار للعين والجلد.
- يتميز نترات الأمونيوم بأنه مركب نشط جداً very reactive
- عامل مؤكسد قوي يسبب حريق مع المواد العضوية والمواد القابلة للاحتراق
- له خواص استرطابية Hygroscopic أي يميل إلى أمتصاص الرطوبة من الهواء
- عند تسخين مركب نترات الأمونيوم تقريباً عند درجة 210 سلزيوس (التفكك الحراري Thermal decomposition) فأنه يتفكك معطياً:
أكسيد النيتروز + أبخرة بيضاء من نترات الأمونيوم + أبخرة بنية من أكاسيد النيتروجين المختلفة NOx + غاز الأمونيا ومعظمها غازات سامة
- نترات الأمونيوم ليست مادة قابلة للأشتعال تحت الظروف العادية ولكنها تدعم أى حريق موجود بإمداده بغاز الأكسجين.
ملصقات المواد الخطرة الخاصة بنترات الأمونيوم
قد تجد واحد أو أكثر من الملصقات الآتية على الحاويات الحاوية لمركب نترات الأمونيوم:
أولاً: ملصقات التصنيف الدولي البحري للبضائع الخطرة IMDG
- ملصق 5.1 المواد المؤكسدة رقم الأمم المتحدة Un1942

ثانياً : ملصق GHS
- GHS وهو النظام العالمي المتوافق لتصنيف وترميز المواد الكيميائية
- ملصق المواد المهيجة + ملصق المواد المؤكسدة

ثالثاً: ملصق NFPA704
- ملصق NFPA704 هو الرابطة الوطنية للوقاية من الحرائق رقم 704
- وهو مقياس يبين نسبة الخطورة على (الصحة - الحريق - الثبات أو الاستقرار ) مدرج من صفر إلى 4 حيث الصفر أقلها خطورة.
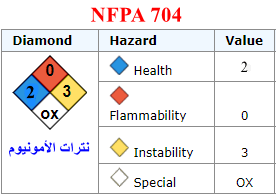
- اللون الأحمر مقياس للاشتعال والعدد (0) يعنى أنها لا تشتعل مثل الماء.
- اللون الأزرق مقياس للصحة والعدد (2) يعنى أنها قد يسبب التعرض الكثيف أو المستمر ولكن غير المزمن إلى فقدان مؤقت للقدرة أو ضرر دائم محتمل.
- اللون الأصفر مقياس للنشاط التفاعلي والعدد (3) يعنى أنها تنحل مع وجود انفجار عند التسخين أو عند درجات حرارة عالية.
طرق مكافحة الحريق المحتوى على نترات الأمونيوم
- نترات الأمونيوم ليست مادة قابلة للأشتعال تحت الظروف العادية ولكنها تدعم أى حريق موجود بإمداده بغاز الأكسجين.
- يستخدم الماء بكميات كبيرة لإطفاء الحرائق الكبري المحتوية على نترات الأمونيوم.
- قد توفر طفاية الهالون أو طفاية غاز ثأنى أكسيد الكربون تحكم فى حريق لمدة قصيرة فى حالة الحريق البسيط.
- لا تستخدم الطفايات التالية: طفاية البودرة الجافة - طفاية الرغوة
- لا تحرك الحاويات المحتوية على نترات الأمونيوم إذا تعرضت للحرارة العادية أو التسخين.
- برد الحاويات المحتوية على حريق نترات الأمونيوم بغمرها بالماء حتى بعد اندلاع الحريق.
- تتم عملية الأطفاء على مسافات كبيرة (خوفاً من الإنفجار المتوقع) أو استخدام اجهزة اطفاء آلية unmanned hose holders
التخزين الآمن لنترات الأمونيوم
- يخزن نترات الأمونيوم فى مكان جاف بارد جيد التهوية في حاويات محكمة الأغلاق.
- يحفظ بعيداُ عن الحرارة العالية والتعرض لرطوبة الهواء أو الماء.
- لا يخزن نترات الامونيوم بالقرب من المواد التالية:
(1) المواد الصلبة القابلة للاحتراق مثل الأقمشة والأوراق والسوائل الهيدروكربونية
(2) الفلزات / المعادن المتواجدة على هيئة بودرة مثل الزنك والنحاس والألومنيوم
(3) المواد المختزلة القوية مثل البرمنجانات
(4) الأحماض القوية مثل حمض النيتريك وتنتج غازات سامة
(5) المركبات الآتية: البرومات Bromates والكلورات Chlorites والهيبوكلورات hypochlorites والبيركلورات perchlorates والنترات nitrites
- أوراق السلامة الخاصة بنترات الأمونيوم
MSDS for Ammonium Nitrate