يوجد ثلاث نظريات لتعريف الحمض والقاعدة وهي:
(1) نظرية أرهينيوس Arrhenius theory
الحمض: المادة التي عند ذوبانها في الماء تتأين مكونه أيونات الهيدروجين الموجبة ( H+)
القاعدة: هي المادة التي تطلق أيونات الهيدروكسيد السالبة (OH-)
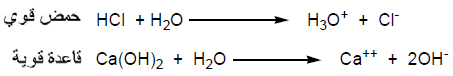
(2) نظرية برونستند – لوري Bronsted - Lowry theory
الحمض على أنه المادة التى تعطي بروتوناً فى محلولها وأن القاعدة هي المادة التى تستقبل ذلك البروتون
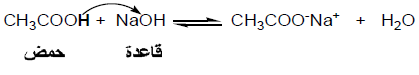
(3) نظرية لويس Lewis theory
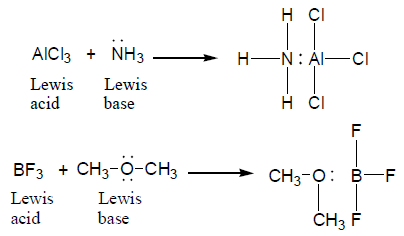
الحمض: المادة التي لها المقدرة على كسب زوج من الإلكترونات وتعتبر اليكتروفيلات (electrophile)
القاعدة: المادة التى لها المقدرة على منح زوج من الإلكترونات وتعتبر نيوكلوفيلات (nucleophile).
- يمكنك قراءة المزيد عن تعريف الحمض والقاعدة باللغة العربية من موقع تعرف على علم الكيمياء وباللغة الأنجليزية من موقع Read chemistry