نوع التهجين في مركب PCl5
(1) نكتب التركيب الإلكتروني لذرة الفسفور في الحالة المستقرة (المنفردة).
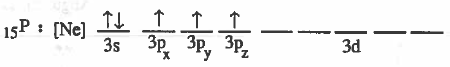
تركيب لويس لجزيء PCl5 هو:
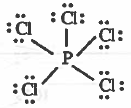
نلاحظ أن حول الذرة المركزية خمسة أزواج إلكترونية رابطة، فأنه حسب نظرية (VSEPR) سوف تتوزع الأزواج الإلكترونية في أركان هرم ثلاثي مزدوج. وهذا يعني أن التهجين من نوع sp3d
وبذلك فنحن في حاجة إلى خمسة مدارات متساوية في الطاقة، كل مدار يحتوي على إلكترون منفرد. ويمكن شرح ذلك كما يلي:
(2) ينتقل (يستثار) إلكترون من المدار (3s) إلى أحد مجالات (3d) الفارغة عندما يكتسب طاقة ليصبح لدينا خمس إلكترونات مفردة.
التركيب الإلكتروني لذرة الفسفور (P) في الحالة المثارة:
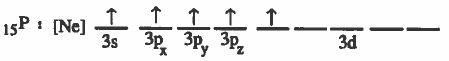
(3) تحـدث عـمـليـة دمج مـدار من نوع (3s) مع ثلاث مـدارات من نوع (3p) ومـدار واحـد من نوع (3d) لنحصل على خمس مـدارات مهجنة من نوع ( sp3d) . ويـحـتـوى كل مـدار منها على إلكترون منفرد.
التركيب الإلكتروني لذرة الفسفور في بعد التهجين:
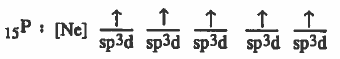
(4) يحدث تداخل بين مـجـال (3p) من ذرة الكلور ومـجـالات (sp3d) المهجنة من ذرة الفسفور لتتكون خمس روابط تساهمـيـة
وحيث أن المركب ينتمي إلى النوع (AX5) إذن الشكل الهندسي لـلـجـزيء هو شكل هرم مثلني مزدوج ( Trigonal bibyramidal ) . وهذا الشكل الهندسي هو الشكل الوحيد الذي يجعل الأزواج الإلكترونية أقل تنافراً.
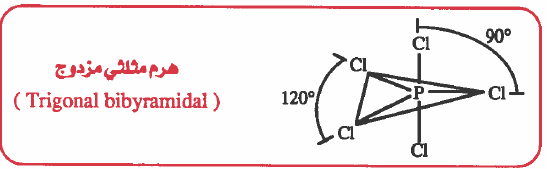
من الأمثلة المشابهة لـ PCl5 في التهجين والشكل الهندسي: SbCl5 & AsF5