توزيع الكاتيونات Cations distribution
- صنفت الكاتيونات الشائعة إلى ست مجموعات وكل مجموعة تمتاز بكاشفها الخاص بها ، والذي يرسب كل الأيونات التي تحتويها، ويسمى هذا الكاشف بكاشف المجموعة Group reagent
- أما الكواشف التي تستعمل أثناء التجارب التأكيدية التي تجرى للتعرف عن أيونات مجموعة ما فهي تسمى بالكواشف النوعية.
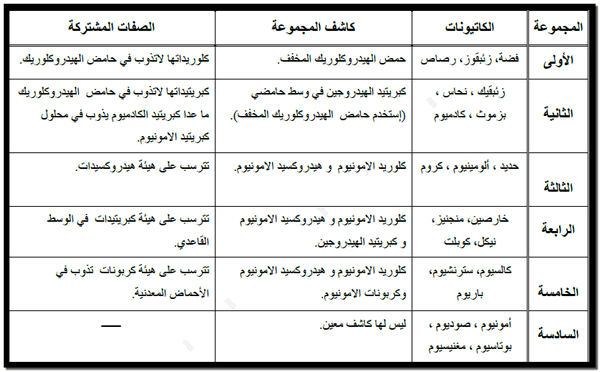
- ويجب الملاحظة أن كاتيونات كل مجموعة لا تتفاعل مع كواشف المجموعة السابقة ولكن يمكن أن تتفاعل مع كواشف المجموعات التالية.
- ويجب إتباع خطوات الكشف كما هو موضح هنا لكي تتم عملية الكشف بنجاح.
(1) قبل الكشف عن كاتيونات أي مجموعة لابد من تنظيف أنابيب الاختبار وهذا باستعمال فرشة تنظيف الأنابيب المستعملة في نهاية كل حصص العملي.
(2) يجب الكشف عن المجموعات الست حسب الترتيب كما يجب إتباع طرق العمل بدقة للحصول على نتائج صحيحة.
(3) ضع في الأنبوبة (Tube) النظيفة محلول العينة وأضف محلول (solution) كاشف المجموعة وإذا لم يحدث أي شئ انتقل إلى المجموعة التالية أما إذا تكون راسب فأجري التجارب التأكيدية مستعملاً جدول الكشف المناسب.
الكشف عن كاتيونات المجموعة الأولى من الشقوق القاعدية
- تشتمل هذه المجموعة على الكاتيونات الآتية: الفضة +Ag ، الرصاص +Pb2 ، الزئبقوز +Hg22
- كاشف المجموعة هو حمض الكبريتيك المخفف HCl
- الصورة الترسيبية : كلوريدات بيضاء اللون وهي:
كلوريد الفضة (راسب أبيض) AgCl
كلوريد الرصاص (راسب أبيض) PbCl2
كلوريد الزئبقوز (راسب أبيض) Hg2Cl2
وتتميز هذه الكلوريدات بأنها لا تذوب فى الماء فيما عدا كلوريد الرصاص يذوب فى الماء الساخن.
جدول الكشف عن كاتيونات المجموعة الأولي
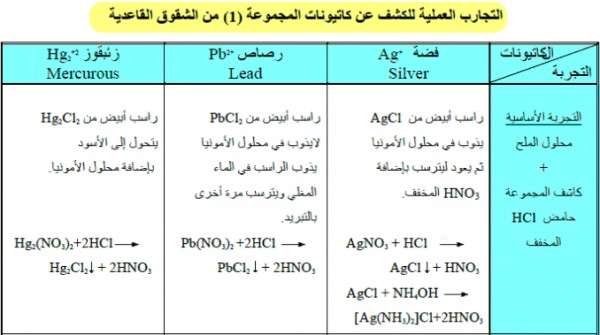
لماذا يكشف HCl المخفف عن كاتيون الفضة في نترات الفضة علي الرغم من أن HCl أقل ثباتاً من الحمض المشتق منه مجموعة النترات؟
- يتم الكشف عن كاتيون الفضة باستخدام حمض الهيدروكلوريك المخفف وذلك لأنه يتكون راسب كلوريد الفضة لا يذوب فى الماء ويذوب فى محلول الأمونيا ثم يعود ليترسب بإضافة حمض النيتريك المخفف ويمكن تمييزه بالتجارب التأكيدية بسهولة.
- الهيدروجين فى حمض الهيدروكلوريك يسبق الفضة فى متسلسلة النشاط الكيميائي لذلك يحل محلها (تفاعل أحلال مزدوج)
AgNO3 + HCl → AgCl↓ + HNO3