التآكل (الصدأ) Corrosion
- من المعروف أن تفاعلات الأكسدة والاختزال التلقائية في الخلايا الجلفانية، حيث تحدث هذه التفاعلات أيضاً في الطبيعة.
- من تفاعلات الأكسدة والاختزال التلقائية هو تآكل الحديد المعروف بالصدأ.
- الصدأ هو خسارة الفلز الناتج عن تفاعل أكسدة واختزال بين الفلز والمواد التي في البيئة.
- على الرغم من الاعتقاد أن الصدأ ناتج تفاعل الحديد مع الأكسجين إلا أنه تفاعل أكثر تعقيدا. ولما كان الصدأ يحدث عند توافر كل من الماء والأكسجين ، لذا فأن قطعة حديد كما فى الشكل التالي التي تركت معرضة للهواء والرطوبة هي أكثر عرضة للصدأ.

- حيث يصدأ الجزء المتصل بالتربة الرطبة أولاً. ويبدأ الصدأ عند وجود شق أو كسر في سطح الحديد. ويصبح هذا الجزء أنود الخلية؛ حيث تبدأ ذرات الحديد في فقدان الإلكترونات:
-Fe(s) → Fe2+(aq) + 2e
كما فى الشكل التالي:
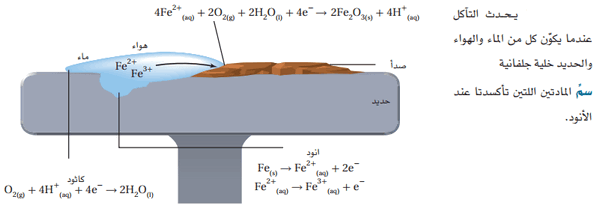
- تصبح أيونات الحديد (II) جزءاً من المحلول المائي، في حين تتحرك الإلكترونات خلال القطعة الحديدية إلى منطقة
الكاثود، وفي الواقع تصبح القطعة الحديدية الدائرة الخارجية والأنود في آن واحد.
- يقع الكاثود عادة على حافة قطرة الماء، حيث يتم الاتصال بين الماء والهواء وقطعة الحديد. وهناك تختزل الإلكترونات الأكسجين من الهواء، كما في المعادلة الآتية:
(O2(g) + 4H+(aq) + 4e- → 2H2O(l
- يتم تزويد أيونات +H على الأرجـح من تكون حمض الكربونيك الناتج عن ذوبان CO2 من الهواء في الماء.
- ثم تتأكسد أيونات الحديد +Fe2 في المحلول إلى أيونات +Fe3 عن طريق التفاعل مع الأكسجين الذائب في الماء.
- تتحد أيونات +Fe3 بالأكسجين لتكوين صدأ غير ذائب من Fe2O3 كالتالي:
(4Fe2+(aq) + 2O2(g) + 2H2O(l) + 4e- → 2Fe2O3(s) + 4H+(aq
عند جمع المعادلات الثلاث تنتج المعادلة الكلية لتفاعل الخلية لتآكل الحديد:
(4Fe(s) +3O2(g) → 2Fe2O3(s
الصدأ عملية بطيئة لأن قطرات الماء تحتوي على كمية قليلة من الأيونات، لذا فهي محاليل موصلة غير جيدة.
- أما إذا كان الماء يحتوي على كمية كبيرة من الأيونات - كما في ماء البحر أو المناطق التي ترش فيها الطرق بالملح شتاءً فإن التآكل يحدث بسرعة أكبر لأن الماء يصبح محلولا ً موصلا ً جيداً.

السؤال: عندما يتعرض مسمار حديد للصدأ هل تزداد كتلته النهائية أم تقل؟ مع ذكر السبب ؟
- عندما تتعرض قطعة من الحديد للصدأ (مسمار مثلاً) فأن كتلة فلز الحديد نفسة تقل وذلك لأن الصدأ هو عملية تآكل لجسم الفلزالناتج عن تفاعل أكسدة واختزال بين الفلز والمواد التي في البيئة أى خسارة فى الوزن.
- على الرغم من أن كتلة فلز الحديد تقل إلا أن الكتلة النهائية للمسمار تزداد نتيجة تكون الصدأ بسبب تحول جزء من فلز الحديد إلى مركب Fe2O3 حيث أن الكتلة المولية لأكسيد الحديد (160 جم) أكبر من الكتلة المولية للحديد (56 جم).
- الحديد المصاب بالصدأ أثقل (نظرياً) من الحديد السليم ، وفي الواقع أن هذه الزيادة صحيحة إذا أمكن ضمان عدم تفتت و اهتراء الطبقات المتأكسدة بتأثير العوامل المحيطة (أي عند عدم وجود فاقد وزني ناتج عن الاهتراء و الاحتكاك لأن الحديد المؤكسد أقل ترابطاً بكثير من الحديد السليم بدون شك).