كلوريد الألومنيوم Aluminium chloride
- كلوريد الألومنيوم هو مركب كيميائي له الصيغة AlCl3 ، ويعد من أحماض لويس القوية
- يتواجد كلوريد الألومنيوم على شكلين:
(1) خالي من الماء ويطلق عليه كلوريد الألومنيوم اللامائي وصيغته الكيميائية AlCl3
(2) مرتبط مع ست جزيئات من الماء؛ سداسي هيدرات كلوريد الألومنيوم AlCl3.6H2O
- يكون كلوريد الألومنيوم اللامائي في شكله النقي على شكل بلورات بيضاء ، إلا أنها تصبح صفراء بوجود آثار من كلوريد الحديد.

- تتميز بلورات كلوريد الألومنيوم اللامائي أنها شغوفة للرطوبة بحيث أنها تدخن بوجود هواء رطب.
الرابطة فى كلوريد الألومنيوم
- الكلور عنصر لا فلزي والألومنيوم عنصر فلزي ومن المتوقع أن تتكون رابطة آيونية ولكن يلعب الفرق فى السالبية الكهربية بين الألومنيوم والكلور دوراً مميزاً فى هذة الحالة.
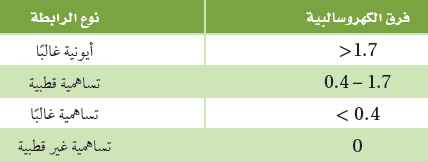
- الجدول التالي يوضح العلاقة بين الكهروسالبية ونوع الرابطة
- الفرق فى السالبية الكهربية بين الألومنيوم (1.5) والكلور (3) يكون 1.5 ولهذا فأن هذا الفرق فى السالبية الكهربية قريب جداً من الحد الفاصل بين الرابطة الأيونية والرابطة التساهمية (1.7).
- وعلى ذلك فأن الرابطة فى كلوريد الألومنيوم تكون رابطة أيونية بخصائص تساهمية عالية جداً.
- الجدول التالي يوضح ارتباط الكلور مع فلزات الصوديوم والماغنسيوم والألومنيوم
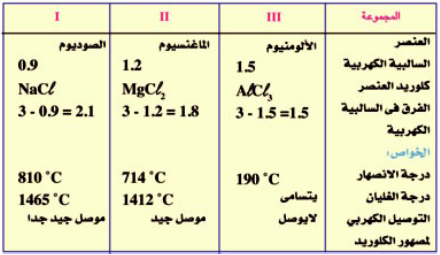
- يتضح من الجدول أنه كلما زاد الفرق فى السالبية الكهربية بين العناصر المرتبطة كلما زادت الخاصية الأيونية.
- وقد ثبت بالتجربة العملية أنه عندما يكون الفرق في السالبية الكهربية أكبر من 1.7 فإن المركب الناتج يكون أيونياً غالباً فمركب كلوريد الصوديوم تتضح فيه تماماً الخواص الأيونية من حيث ارتفاع درجتى الانصهار والغليان وجودة التوصيل الكهربي.
- بعكس مركب مثل كلوريد الألومنيوم الذي تظهر فيه خواص الرابطة التساهمية أكثر من الرابطة الأيونية حيث تكون خصائص الرابطة الأيونية فى كلوريد الألومنيوم 43% وخصائص الرابطة التساهمية 53%
- الدليل على ذلك هو أن مصهور كلوريد الألومنيوم لا يوصل التيار الكهربي.