قانون بويل للغازات Boyles,s Law
- ضغط الغاز وحجمه مترابطان. وقد وصف العالم الإيرلندي روبرت بويل هذة العلاقة.
- قانون بويل هي علاقة تربط بين ضغط الغاز وحجمه.
كيف يرتبط الضغط مع الحجم
- صمم بويل تجربة كالموضحة فى الشكل التالي:

- وضح بويل من خلالها أنه إذا كانت كمية الغاز ودرجة الحرارة ثابتتين فإن مضاعفة الضغط الواقع على الغاز يقلل من حجمه إلى النصف. ومن ناحية أخرى فإن تقليل الضغط الواقع على الغاز إلى النصف يضاعف حجم الغاز.
- لذلك لاحظ بويل أن حجم الغاز يقل كلما زاد الضغط المسلط عليه والعكس صحيح وذلك عند تثبيت درجة الحرارة وكمية الغاز.
نص قانون بويل
يتناسب حجم الغاز عكسياً مع الضغط المسلط عليه عند ثبوت درجة الحرارة وكمية الغاز
الشكل الرياضى لقانون بويل
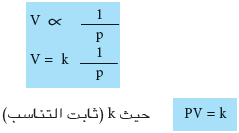
- أى أن حاصل الضرب للضغط والحجم بأية حال يساوي كمية ثابتة.
- عند أخذ عينة من غاز ذات حجم V1 تحت ضغط P1عند درجة حرارة ثابتة وقمنا بتغيير ظروف هذا الغاز ليصبح حجمه V2 وضغط P2 مع الاحتفاظ بدرجة الحرارة ثابتة T1 فأنه طبقا لقانون بويل يصح أن نقول:
عند ثبوت الحرارة وكمية الغاز
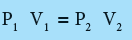
علاقة قانون بالتنفس
- أنت تتنفس 20 مرة فى الدقيقة وتستبدل بغاز ثاني أكسيد الكربون غاز الأكسجين لتحافظ على حياتك فكيف يتغير الضغط والحجم فى رئتيك في أثناء تنفسك؟
التحليل
يسمح النسيج الإسفنجي المرن الذي تتكون منه الرئتان بتمدد الرئتين وانقباضهما ، لتستجيب لحركة الحجاب الحاجز وهو العضلة القوية الموجودة اسفلهما.
- عندما يتحرك الحجاب الحاجز إلى اسفل يزداد حجم الرئتين وبذلك نتمكن من الشهيق.
- كما يتقلص حجم الرئتين عندما يتحرك الحجاب الحاجز إلى أعلى وبذلك نتمكن من الزفير.
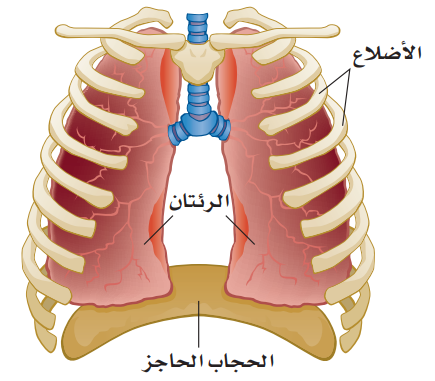
الإجابة: عمليتي الشهيق والزفير في التنفس تطبيق على قانون بويل