حسابات المعادلات الكيميائية Chemical Equations Calculations
- تتحد الذرات أو الجزيئات أو الأيونات مع بعضها بنسب عددية بسيطة في المعادلة الكيميائية الموزونة.
مثال توضيحي (1):
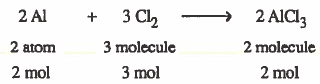
مما سبق نلاحظ أنه يمكن قراءة المعادلة بطريقتين :
- 2 ذرة (Al) تتفاعل مع 3 جزيئات (Cl2) لإنتاج 2 جزيء (AlCl3)
- 2 مول من نرات Al تتفاعل مع 3 مول من جزيئات Cl2 لإنتاج 2 مول من جزيئات AlCl3
مثال توضيحي (2):
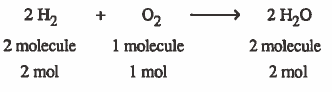
مما سبق نلاحظ أنه يمكن قراءة المعادلة بطريقتين :
- 2 جزيء H2 تتفاعل مع 1 جزيء O2 لإنتاج 2 جزيء H2O
- 2 مول من جزيئات H2 تتفاعل مع 1 مول من جزيئات O2 لإنتاج 2 مول من جزيئات H2O
ملاحظات هامة
لحل الحسابات التي تعتمد على المعادلة الكيميائية يجب:
(1) كتابة المعادلة الرمزية الموزونة.
(2) معرفة نسب مولات المواد الداخلة في التفاعل والناتجة عنه في المعادلة الموزونة من المعاملات الموجودة أمام المواد المتفاعلة والناتجة.
(3) يفضل تحويل الكميات المعطاة في السؤال إلى مولات ليسهل التعامل معها.
مسائل محلولة
مثال (1): احسب عدد مولات الهيدروجين اللازمة للتفاعل مع 42g من النيتروجين حسب المعادلة:
3H2 + N2 → 2NH3
الأوزان الذرية : 14 = H = 1 , N
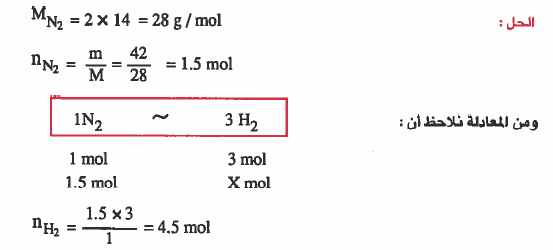
مثال(2): احـسـب عـدد جزيئات (H2O) الناتجة من تفاعل 0.006mol من النشادر حسب المعادلة التالية: (تسخين فوق السهم)
4NH3 + 5O2 → 4NO + 6H2O
الحل:
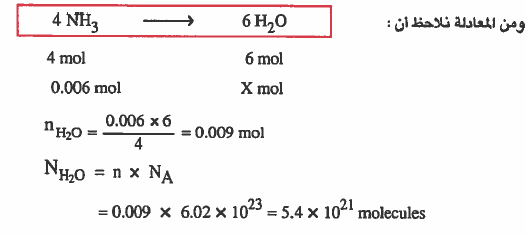
مثال (3): احـسب وزن (Al2O3) الناتج من احـتـراق 135g عن (Al) في جـو من الأكسجين (O2) حسب التفاعل التالي:
3Al + 3O2 → 2Al2O3
الأوزان الذرية :16 = Al = 27, O
الحل:

مثال (4): في وفرة من الاكسجين (O2) احسب عـدد جزيئات بخار الماء الناتجة من احتراق ( molecules 6.02 × 1023 ) من النشادر (NH3) حسب المعادلة التالية: (تسخين فوق السهم)
4NH3 + 5O2 → 4NO + 6H2O
الحل:
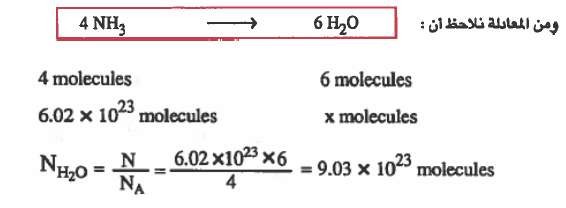
مثال (5): احسب وزن ZnCl2 الناتج من تفاعل ( x 102 formula unit 9.03 ) ـ كبريتيد الخارصين ZnS مع كمية كافية من HC1
ZnS + 2HCl → ZnCl2 + H2S
الأوزان الذرية : 65.4 = C1 = 35.5 , Zn
الحل :
