حرارة التكوين Heat of Formation
- تعریف حرارة التكوين: هي كمية الحرارة المنطلقة أو الممتصة عن تكوين مول واحد من المادة من عناصره الأولية ، بحيث تكون العناصر في حالتها القياسية.

وقد توصل العلمـاء إلـى قيم حـرارة التكوين (انثالبي التكوين) لآلاف المواد ووضعت في جداول.
- ويمكن كتابة معادلة التكوين لإي مادة بشروط:
(۱) المادة الناتجة هي فقط مول من المادة المراد إيجاد حرارة التكوين لها.
(۲) المواد المتفاعلة هي العناصر المكونة للمادة المراد إيجاد حرارة التكوين لـهـا.
بشرط ان تكون هذه العناصر في الحالة القياسية .
سؤال : ماذا نقصد عندما نقول ان العناصر في حالتها القياسية ؟
جواب : نقصد بذلك أن العناصر في حالتها الطبيعية ، فمثلا الأكسجين في حالته الطبيعية يكون جزيئاته ثنائية الذرة في الحالة الغازية (g) O2 اما الكربون فيكون في الحالة الصلبة (s)C ، والكالسيوم في الحالة الصلبة (Ca(s ، والهيدروجين في الحالة الغازية (H2 (g والكلور يكون في الحالة الغازية Cl2(g) والحديد في الحالة الصلبة (Fe (s وهكذا .
فمثلاً لا يمكن استخدام التفاعل التالي لحساب حرارة التكوين لـ CO
C(g)+1/2 O2 (g) → CO (g)
وذلك لأن الكربون في حالته الطبيعية يكون في حالة صلبة وليست غازية.
لاتنسى أن جزيئات العناصر ثنائية الذرة هي فقط:
هيدروجين (H2) ، أكسجين (O2) ، نيتروجين (N2) ، فلور (F2) ، کلور (Cl2) ، بروم (Br2) ، يود (I2)
أمثلة توضيحية على حرارة التكوين

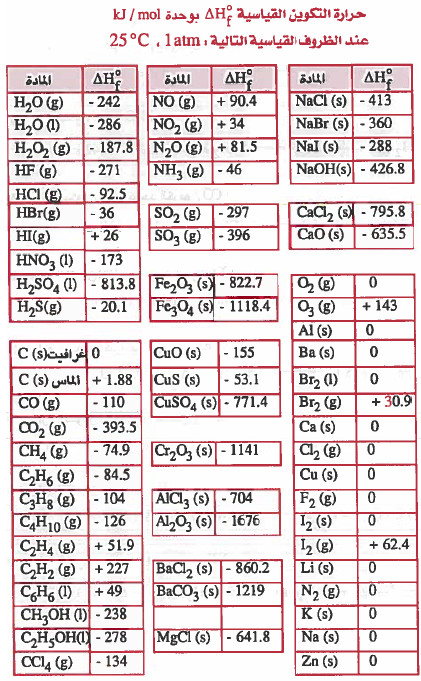

ملاحظات هامة على جدول حرارات التكوين السابق.
(1) حرارة تكوين العناصر النقية تساوي صفر عند كل الدرجات ، ومن الأمثلة على العناصر التالية:
...... , Cu , N2 , Fe , O2 , Na , Cl2 , Hg
(2) معظم حـرارات التكوين سـالـبـة وهذا يعني أن تكوين المركب من عناصره الأوليـة طارد للحرارة.
(3) المركبات التي يصاحب تكوينها طرد للحرارة تكون أكثر استقراراً (علل) وذلك لأن المحتوى الحراري للمركب الناتج أقل من مجموع المحتويات الحرارية للعناصر الداخلة في تركيبه مثل: CH4 , CH3OH
(4) كلما زادت الطاقة المنطلقة زاد ثبات المركب (يصعب تفككه)
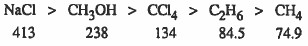
(5) كلما زادت الطاقة الممتصة (المستهلكة) قل ثبات المركب (سهل تفككه)
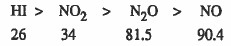
القانون الرياضي لحساب حرارة التكوين
طاقة التفاعل ( التغير الحراري ) = مجموع طاقات تكوين النواتج - مجموع طاقات تكوين المتفاعلات
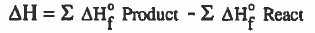
تذكر أن:
M = الوزن الجزيئي (الكتلة المولية )
n = عدد المولات
m = الوزن بالجرام
كتلة مول واحد أو الكتلة المولية = الوزن الجزيئي أو الكتلة الجزيئية