مسائل محلولة على المحاليل المنظمة
مثال (1): أحسب الاس الهيدروجيني pH للمحلول المنظم المكون من: 0.115M NaF + 0.215M HF
علماً بأن : Ka (HF) = 7.0 x 10-4
الحل:
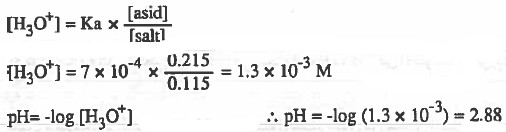
مثال (2): حضر محلول منظم بخلط 0.24M من محلول NH3 و 0.18M من NH4Cl فإذا كان 5-10 × 1.8 = Kb فاحسب الـ pH, pOH لهذا المحلول.
الحل:
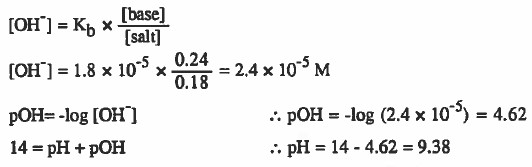
مثال (3): أحسب الرقم الهيدروجيني لمحلول منظم حُضر من حجمين متساويين من (0.2M) حمض البروبانويك و (0.2M) بروبانات الصوديوم.
علماً بان ثابت تأين حمض البروبانويك: (5-10 Ka = 1.34 x) .
الحل:
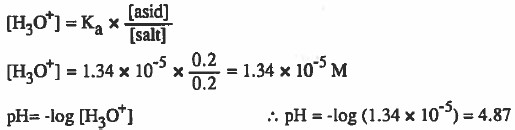
مثال (4): احسب تركيز (NaClO) اللازم إضـافـتـه إلى محلول 0.05M مـن حمض (HClO) ليـتـم الـحـصـول على محلول منظم له 8 = pH مـعـتـبـراً أن ثابت تفكك الحمض يساوي (Ka = 2.9 × 10-8)
الحل:
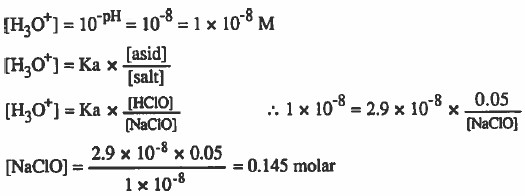
مثال (5): محلول حجمه (200mL) يحتوي على ( 0.028mol) من حمض ضعيف (HB) و (0.007mol) من ملحـه (NaB) فكانت الـ pH للمحلول (3.66) فما هو ثابت التأين للحمض (Ka) .
الحل:

مـثـال(6): احسب الرقم الهيدروجيني (pH) لمحلول منظم من (0.1M) مـن حمض الخل و (0.2M) من خلات الصوديوم قبل وبعد إضافة:
(1) ( 0.01mol HCl) إلى اللتر من المحلول.
(2) ( 0.01mol NaOH) إلى اللتر من المحلول.
علماً بأن : (5-10 × 1.8 = Ka)
الحل:

