تجارب عملية لشرح خواص البنزين
(1) البنزين لا يضم إليه البروم من ماء البروم
- أضف إلى أنبوب اختبار تحتوى على (3) قطرات من ماء البروم و (3) قطرات من البنزين.
- وبما أن البنزين أخف من الماء ولا يذوب فيه فإذا خضضت مزيج البنزين مع الماء وتركته ليركد وجدت أن البنزن يطفو إلى الأعلى وأن لون ماء البروم قد زال .
- غير أن زوال لون ماء البروم لا يفسر بانضمام البروم إلى الروابط الثنائية في حلقة البنزين كما يحصل مع الاثيلين وإنما يفسر يسهولة ذوبان البروم في البنزين أكثر من الماء مما يؤدي إلى انتقاله إلى طبقة البنزين ملونا إياه باللون الأصفر.
- وهكذا فإن البنزين والهيدركربونات العطرية الأخرى دون النظر إلى احتوائها على ثلاثة روابط ثنائية تختلف اختلافاً كبيراً عن (المركبات الأليفاتية) غير المشبعة فهي لا تضم البروم إليها في مواضع انفصام الروابط الثنائية.
ووفقاً للتصورات الحديثة فيمكن تفسير خواص البنزين والهيدركربونات العطرية الأخرىبأن جزيئاتها ليست حاوية روابط أحادية أو ثنائية عادية بل إن الكثافة الالكترونية في جميع الروابط C-C الموجودة في جزيئة البنزين موزعة بالتساوي .
- ولهذا فإن برومة البنزين تجري بصورة مشابهة لبرومة الهيدركربونات المشبعة حيث يجري استبدال ذرة الهيدروجين بذرة بروم وينطلق بروميد الهيدروجين.
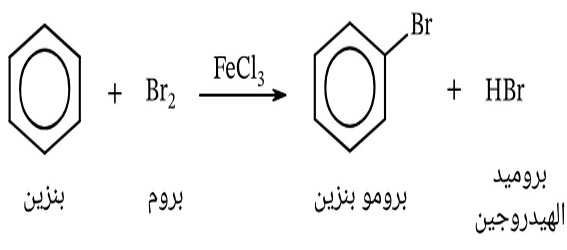
- ويجري هذا التفاعل الأخير في شروط خاصة وبوجود وسائط مناسبة مثل FeCl3
- وفي الشروط العادية نجد أن تفاعل البروم يجري ببطء شديد.
(2) البنزين لا يتأكسد بمحلول برمنجنات البوتاسيوم
خذ أنبوب اختبار تحتوى على (5) قطرات من الماء ، وأضف إليه قطرة من محلول 0.1N من بر منجنات البوتاسيوم KMnO4، وقطرة من محلول 2N من حمض الكبريتيك H2SO4.
- أضف إلى المحلول الناتج قطرة بنزين ورج الأنبوب .
- لا يلاحظ زوال لون برمنجنات البوتاسيوم . وتعد هذه الخاصة مميزة فقط للبنزين الخالي من أقرانه .
- ولتنقية البنزين يلجأ إلى باورته بإحاطة الوعاء الذي عليه بماء يحتوى على الجليد شرط أن تكون (درجة انصهار البنزين 5.5o+ ) فيتجمد البنزين ويمكن لذلك فصله عن الشوائب التي بقيت سائلة .
- وبعد إعادة عملية التبلور مرتين أو ثلاثاً تجري عملية تنقيته كيميائياً بخضه مع حمض الكبريتيك المركز عدة مرات إلى أن يتوقف ظهور التلون في حمض الكبريتيك المستعمل في تنقية أخيرة.