العدد الكتلي Mass number
العدد الكتلي هو مجموع عدد البروتونات (العدد الذري) وعدد النيوترونات في نواة العنصر.

مثال
- العدد الكتلي للأكسجين 16
- العدد الكتلي للألومنيوم 27
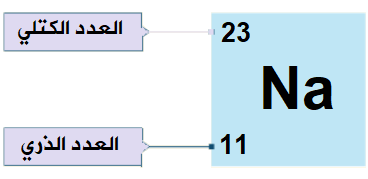
العلاقة بين العدد الذري والعدد الكتلي
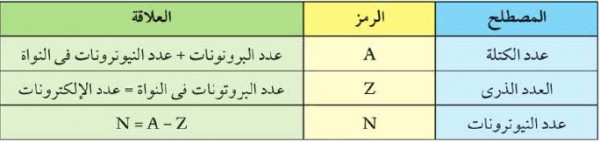
النظائر والعدد الكتلي
- كان جون دالتون مخطئًا عندما اعتقد أنه لا يمكن تجزئة الذرات، وأن ذرات العنصر الواحد متشابهة
- وذلك أن ذرات العنصر الواحد لها نفس عدد البروتونات وعدد الإلكترونات، إلا أن عدد النيوترونات قد يختلف.
- مثال هناك ثلاثة أنواع من ذرات البوتاسيوم موجودة فى الطبيعة ، ويحتوي كل نوع منها على 19 بروتونًا و 19 إلكترونًا، بينما يحتوي أحد أنواع ذرة البوتاسيوم على 20 نيوترونًا، والآخر على 21 نيوترونًا، والثالث على 22 نيوترونًا. تسمى الذرات التي لها عدد البروتونات نفسه لكنها تختلف في عدد النيوترونات بالنظائر.
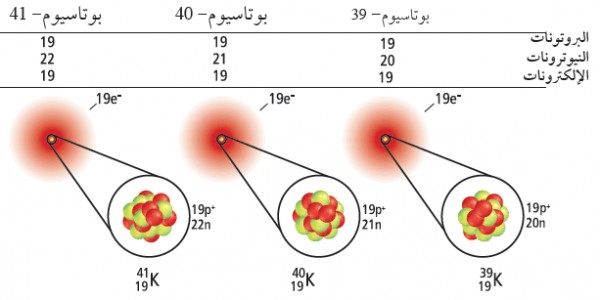
- النظائر: هي الذرات التى لها نفس عدد البروتونات والألكترونات ولكن تختلف فى عدد النيترونات.
- تعريف آخر النظائر هي الذرات التى لها نفس العدد الذري وتختلف فى العدد الكتلي.
- نظائر عنصر الأكسجين

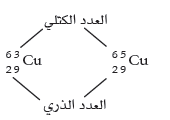
كتلة النظائر
- النظائر التي تحتوي على عدد أكبر من النيوترونات تكون كتلها أكبر.
- على الرغم من هذه الاختلافات إلا أن ذرات نظائر العنصر يكون لها السلوك الكيميائي نفسة وذلك لأن السلوك الكيميائي يحدده فقط عدد الإلكترونات الموجودة في الذرة.