كيفية إيجاد ثابت الاتزان (Kc) بمعلومية التراكيز عند الاتزان
مثال (1): يمكن تحضير الكحول الميثيلي CH3OH عند °700C حسب التفاعل التالي:
CO (g) + 2 H2 (g) = CH3OH (g)
ولقد وجد أن تراكيز المواد عند حالة الاتزان:
CH3OH] = 0.05 M , [CO] = 0.03 M , [H2] = 0.075 M]
أحسب ثابت الاتزان Kc للتفاعل ثم احسب Kp .
الحل:
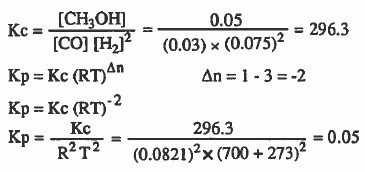
مثال (2): سخنت كمية من PCl5 في وعاء سعته 12L ووجد أن الوعاء يحتوي عند الاتزان على 0.21mol من PCl5 و 0.32mol من PCl3 و 0.32mol من Cl2 احـسـب ثابت الاتزان لتفكك PCl5 عند °250C حسب المعادلة التالية:
PC15 = PCl3 + Cl2
الحل:
نلاحظ انه لم يعطي تراكيز المواد عند الاتزان ، لذا يجب إيجادها كما يلي :

ويمكن اختصار حل السؤال كما يلي:
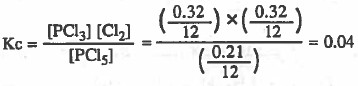
مثال (3): عند درجة °500C حدث التفاعل التالي:
3H2 + N2 = 2NH3
فـإذا وجـد فـي الـوعـاء عند الاتزان 0.25M من H2 و 0.05M من NH3 احـسـب ـتـركـيـز النيتروجين N2 علماً بأن ثابت الاتزان (Kc) يساوي 0.06
الحل:
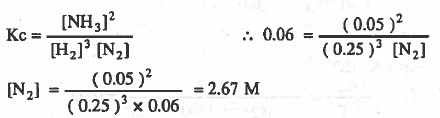
مثال (4): في خليط متزن من ( NH3, H2, N2 ) في إناء سعته 5L عند °500C وجد أن الضغوط الجزئية للمواد كانت:
NH3 = 142.25 atm , H2 = 142.25 atm, N2 = 47.5 atm
أحسب ثابت الاتزان Kc حسب التفاعل:
N2 (g) + 3 H2 (g) = 2 NH3 (g)
الحل:
