حمضية الفينول Acidity of Phenol
- يتميز كل من الفينولات والكحولات بوجود مجموعة هيدروكسيل.
- وقد رأينا أن الكحولات تدخل في تفاعلات تتضمن انفصام الرابطة بين الهيدروجين والأكسجين في مجموعة الهيدروكسيل ولكنها تتصف بحمضية ضعيفة.
- وبالمثل فإن الفينولات تتصف بالحمضية ولكنها أقوى من حموضة الكحولات.
- فالمحلول المائي للفينول حقاً حمضي تجاه ورقة عباد الشمس، وتذوب الفينولات في محلول هيدروكسيد الصوديوم وتكون أملاحاً تعرف بالفينوكسيدات.
- وتعزى زيادة الحموضة عند الفينولات، مقارنة بالكحولات إلى عاملين هما التأثير التحريضي Inductive effect والتأثير التأرجحي Resonance.
أولاً/ التأثير التحريضي Inductive effect
- ترتبط مجموعة هيدروكسيل الكحول بذرة كربون sp3 في حين أن مجموعة هيدروكسيل الفينول مرتبطة بذرة كربون sp2 ولما كانت ذرة كربون sp2 أكثر سالبية كهربية من ذرة كربون sp3 فإن ذلك من شأنه زيادة الحموضة عند الفينولات نتيجة التأثير التحريضي Inductive effect حيث أن ذلك يؤدى إلى زيادة ثبات القاعدة المرافقة (أيون الفينوكسيد).
- بمعنى آخر فإن أي ذرة مرتبطة بالمجموعة الألكيلية ستكون متخمة بالالكترونات فأي بروتون مرتبط بهذه الذرة سيكون من الصعب إزاحته، وعليه فالمجموعة الألكيلية في الكحولات ستكون عاملاً ذو تأثير على ضعف حمضية الكحول وفي نفس الوقت ستكون ذو تأثير على زيادة قاعديته:
CH3-OH , Ka = 10-16
Phenol , Ka = 1.3 x 10-10
ثانياً/ التأثير التأرجحي Resonance
- وإذا ما نظرنا إلى الأشكال التأرجحية في جزىء الفينول أو أيون الفينوكسيد فإنه يتضح لنا عدم تمركز الشحنة السالبة حيث تتوزع على ذرات كربون الحلقة الأروماتية.
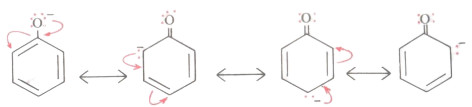
- وهذه الأشكال التأرجحية تؤدي إلى ثبات أيون الفينوكسيد (القاعدة المرافقة للفينول) وعليه فهو قاعدة ضعيفة، مقارنة بالألكوكسيد (في الكحولات) حيث أنه في أيون الألكوكسيد فإن الشحنة السالبة متمركزة على ذرة الأكسجين.
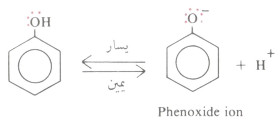
«أكثر ثبات»، لذلك الاتزان يكون ناحية اليمين مما يزيد من حمضية الفينول.
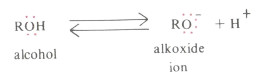
«أقل ثبات لذلك الاتزان يكون أقل ناحية اليمين من السابق مما يقلل من حمضية الكحول مقارنة بالفينول.
حامضية مشتقات الفينول
- تزداد حموضة مشتقات الفينول مقارنة بالفينول نفسه
- عند وجود مجموعات ساحبة للالكترونات على الحلقة الأروماتية إذ تعمل هذه المجموعات على ثبات أيون الفينوكسيد.
- وعلى العكس من ذلك فإن وجود مجموعة معطية للالكترونات على الحلقة يؤدي إلى عدم ثبات أيون الفينوكسيد الذي يترتب عليه ضعف حموضة مشتق الفينول
- ويتضح ذلك من الجدول التالي الذي يبين (Ka) البعض الفينولات
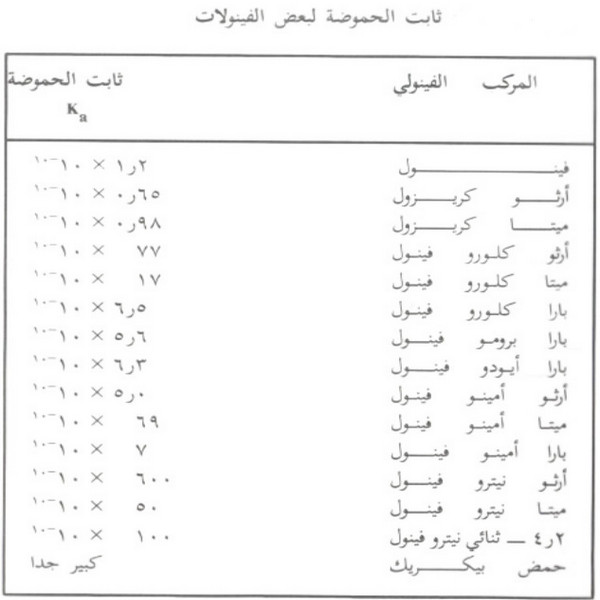
- تذوب الفينولات في هيدروكسيد الصوديوم وتتحول إلى أملاح الصوديوم الذوابة في الماء.
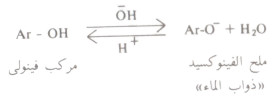
- وهذا التفاعل عكسي، فإضافة الزيادة من الحمض يرجع الملح إلى الفينول المطابق.
- ولا تذوب الفينولات في القواعد الضعيفة مثل بيكربونات الصوديوم إلا الفينولات التي تحوي أكثر من مجموعة ساحبة مثل ثنائي نيتروفينولات فهذه فينولات لها صفة حمضية تقارن بالخاصية الحمضية للحموض الكربوكسيلية.
- وعموماً فإن إمكانية ذوبان الفينولات في المحاليل المائية للقواعد القوية يوفر أسلوباً جيداً لدارس الكيمياء العضوية لفصل الفينولات فيما لو وجدت في خليط مع كثير من المركبات العضوية.
- فعلى سبيل المثال لو وجد خليط من الفينول وكلورو بنزين فإنه يمكن فصلهما عن بعض باستخدام محلول مائي من قاعدة قوية مثل هيدروكسيد الصوديوم حيث ينفصل الأول على هيئة ملح في الطبقة المائية.
- وتجري هذه التجربة في المختبر بإذابة الخليط في مذيب عضوي لا يمتزج مع الماء مثل الايثر أو ثنائي كلورو ميثان.
- ومن ثم يتم استخلاص الفينول بإضافة المحلول المائي للقاعدة حيث يذوب الفينول ويتحول إلى ملح الفينوكسيد الذائب في الطبقة المائية بينما يبقى كلورو بنزين في الطبقة العضوية.