التمييز بين الأحماض القوية والضعيفة والقواعد القوية والضعيفة
(1) يجب عليك أولاً فهم موضوع الأحماض والقواعد جيداً.
(2) بعد الممارسة والتعامل معها باستمرار سيتكرر أمامك أشهر الأحماض والقواعد ومدى قوتها او ضعفها.
(3) استخدم الأنترنت للتفرقة بين حمضين أو قاعدتين وذلك من خلال pKa , pKb
كلما كانت pKa أقل كلما كانت Ka أكبر وكان الحمض قوياً والعكس صحيح.
كل ما عليك أن تكتب باللغة الأنجليزية في جوجل مثلاً :
pKa for Acetic acid
ستظهر لك قيمة pKa للحمض وكذلك أفعل نفس الشئ للأحماض الأخرى وقارن بينها عن طريق تلك القيم.
مثال :

أولاً : الأحماض Acids
الأحماض القوية Strong acids
- هي الأحماض التي تتأين بشكل كلي في الماء، وينتج من هذا التأين أيونات موجبة وأخرى سالبة، وتكون موصلة للكهرباء بكفاءةٍ عالية.
- ومن الأمثلة على الأحماض القويّة:
(1) حمض الهيدروكلوريك HCl
(2) حمض النتريك HNO3
(3) حمض الكبريتيك H2SO4
(4) حمض البيركلوريك HClO4
(5) حمض بروميد الهيدروجين HBr
(6) حمض يوديد الهيدروجين HI
الأحماض الضعيفة Weak acids
- هي الحموض التي تتأين بشكلٍ جزيءّ في الماء، وتكون موصلة للكهرباء بشكلٍ ضعيف.
- ومن الأمثلة على الحموض الضعيفة:
(1) حمض الأستيك CH3COOH
(2) حمض الهيدروفلوريك HF
ثانياً: القواعد Bases
القواعد القوية Strong base
- هي القواعد التى تتأين بشكل تام في محاليلها المائية.
- ومن الأمثلة على القواعد القوية:
(1) هيدروكسيد الكالسيوم Ca(OH)2
(2) هيدروكسيدات المجموعة الأولي مثل: NaOH , KOH , LiOH
القواعد الضعيفة Weak base
- هي القواعد التى تتأين جزئياً في محاليلها المائية.
- ومن الأمثلة على القواعد القوية:
(1) الأمونيا NH3 ومشتقاتها (الأمينات العضوية)
(2) الهيدرازين N2H4 ومشتقاتها.
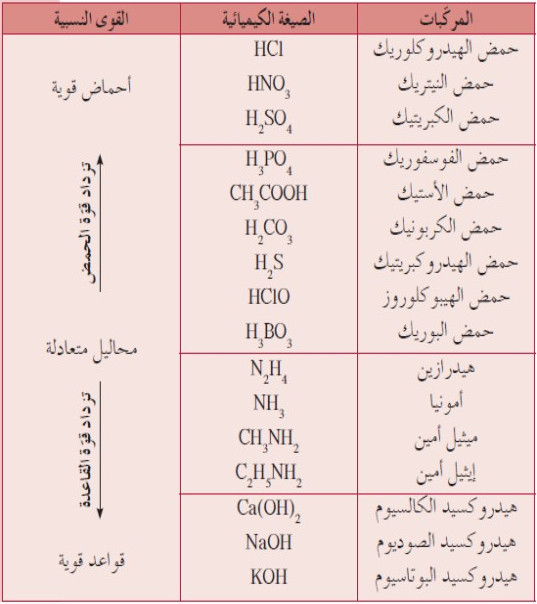
الجدول التالي يوضح أشهر الأحماض والقواعد ومدى قوتها