التهجين فى الجزئيات المكونة من أربع ذرات
إذا كان الجزيء مكون من 4 ذرات فهناك حالتين للتهجين :
الحالة الأولى: إذا كانت الذرات متماثلة P4
فيكون شكل الجزيء رباعى منتظم الأوجة ولا يكون عزم مغناطيسي . ويكون نوع التهجين SP3
الحالة الثانية : إذا كانت الذرات مختلفة AB3
وتنقسم إلي :
(1) إذاكان التهجين SP3 كما في NH3 / PH3 / AsH3 ويكون شكل الجزيء رباعى الأوجة فيه الثلاث ذرات B3 علي شكل مثلث مستوى والذرة A تشغل قمة الهرم المثلثى ولذا للجزيء عزم قطبى مزدوج لأن السحابات الإلكترونية تتجه إلي الذرة الأكثر سالبية .
(2) إذا كان التهجين SP2 : كما في BCl3 فإن الثلاث ذرات B3 تشكل مثلث مستوى وتقع الذرة في مركز ثقل المثلث ويكون الجزيء مستوى وليس له عزم قطبى مغناطيسي .
التهجين فى ASH3
As33 = [Ar]18 4S2 3d10 4P3
AsH3 : 5 + 3 x 1 = 8e
8e / 2 = 4 = SP3
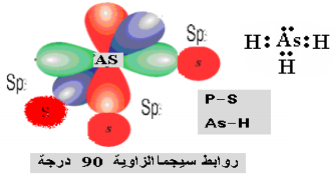
- الأفلاك التى شكلت الروابط هي أفلاك 4P من الزرنيخ (As) مع الفلك S من الهيدروجين.
- بما أن الزاوية 90o فهذا يعني أن As استخدمت في تكوين الروابط اأفلاك ذرية بسيطة ولم تستخدم أفلاك ذرية مهجنة من نوع SP3.
- ولا يلزم تهجين S مع P لأن الزاوية المحصورة تشير إلى عدم حاجة ذرة AS لعملية التهجين وكبر حجم ذرة As الذي أدي بدوره إلى زيادة حجم أفلاك 4P أدى إلى عدم حاجة ذرة AS التهجين.