تعدد حالات تأكسد العناصر الأنتقالية
- فيما يلى حالات التأكسد لعناصر السلسلة الأنتقالية الأولي
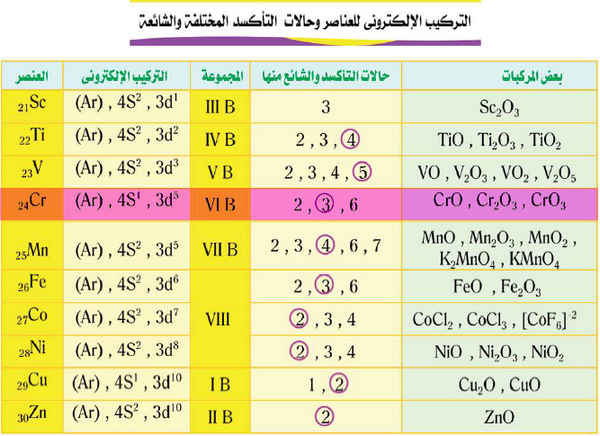
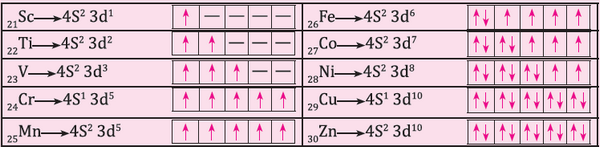
- ملحوظة هامة : الأمتلاء الكامل أو النصفي للمستوى الفرعي ليس هو العامل الوحيد لثبات التركيب الإلكتروني للعنصر فى المركب.
- فلو كان الإمتلاء الكامل أو النصفي للمستوى الفرعي هو العامل الوحيد لثبات العنصر فيكون بذلك الكروم والنحاس عناصر خاملة لن تدخل فى التفاعلات الكيميائية وهذا لن يحدث وغير موجود.
حالات تأكسد الكروم
- حالات التأكسد الممكنة للكروم هي +2 , +3 , +6
- من مركبات الكروم (+2) هو Chromium (II) oxide CrO
- من مركبات الكروم (+3) هو Chromium (III) oxide Cr2O3
- من مركبات الكروم (+6) هو Chromium (VI) oxide CrO3
- حالة التأكسد (+3) هى الأكثر شيوعاً وذلك لأنها أفضل من ناحية الطاقة
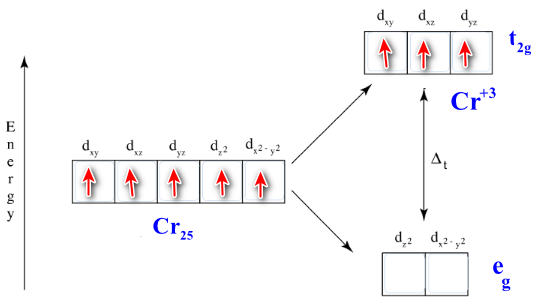
لماذا تكون حالة التأكسد +3 للكروم هى الأكثر شيوعاً
فى حالة التأكسد (+3) يفقد الكروم إلكترون من المستوى الفرعي (4s) وإلكترونين من المستوى (3d) ليصبح المستوى الفرعي (3d) يحتوى على ثلاث إلكترونات فقط.
- تنقسم المستوى الفرعي (d) إلى خمس مدارات غير متمائلة حسب نظرية المجال البلوري CFT وهي:
(1) مدارات t2g والتى توجه فيها فصوص المدار(d) بين المحاور (x , y , z) وهي dx-y , dx-z , dy-z
(2) مدارات eg وفيها توجة الفصوص على طول المحاور وهي dx2-y2 , dz2
- يكون المدارات t2g نصف ممتلئة وهى أفضل من ناحية الطاقة والأستقرار