أولاً: حساب عدد مولات هيدروكسيد الصوديوم
حساب عدد مولات هيدروكسيد الصوديوم
1mol → 40 gm
mol → 13.9 gm??
عدد مولات هيدروكسيد الصوديوم = 0.35 مول
ثانياً: حساب كمية الطاقة المنطلقة
حرارة الذوبان المولارية Molar heat of solution: هي مقدار التغير الحراري الناتج عن ذوبان مول من المذاب في كمية من المذيب لتكوين لتر من المحلول.
- إذا كانت كمية المادة المذابة لا تساوي 1 مول يمكن حساب حرارة الذوبان المولارية من العلاقة:
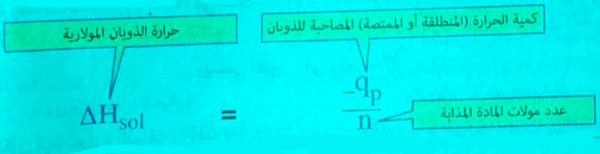
وبالتعويض فى المعادلة:
44.4 = q/0.35
كمية الحرارة المنطلقة = 15.4 كيلو جول = 15400 جول
ثالثاُ: حساب قيمة t2
من قانون التبادل الحراري التالي يمكن حساب درجة الحرارة t2
كمية الحرارة (q) المفقودة من هيدروكسيد الصوديوم = - كمية الحرارة (q) المكتسبة بواسطة الماء
= M * S * Δt
15400 = 250 * 4.18 * (t2-t1)
15400 = 250 * 4.18 * (t2-23)
15400 = 1045t2 - 24035
t2 = 37.7
هذا والله أعلم