جهد التأين (طاقة التأين) Ionization energy
مقدار الطاقة اللازمة لإزالة أو فصل أقل الإلكترونات ارتباطاً بالذرة المفردة وهى في الحالة الغازية.
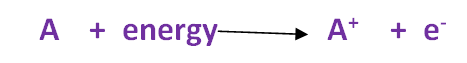
ملاحظات هامة على جهد التأين
(1) جهد التأين ماص للحرارة ( + )
(2) قد يوجد للعنصر أكثر من جهد تأين لأنه من الممكن إزالة إلكترون أو أثنين أو ثلاثة من الذرة فقد يوجد للذرة جهد تأين أول وثان وثالث.... الخ
(3) جهد التأين الأول للغازات النبيلة مرتفع جداً لإستقرار نظامها الإلكتروني حيث يصعب إزالة إلكترون من مستوي طاقة مكتمل
(4) جهد التأين الثاني أكبر من جهد التأين الأول وذلك لزيادة شحنة النواة عن شحنة الألكترونات المتبقية فى الذرة مما يزيد من قوة جذب النواة للإلكترونات
(5) الجهد الـتأين الثالث يكون أكبر من جهدى التأين الأول والثاني وذلك لأنه قد يتسبب فى كسر مستوى طاقة مكتمل كما فى ذرة الماغنسيوم

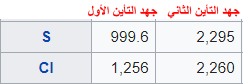
التوزيع الألكتروني للكبريت والكلور
Cl17 : 1s2 , 2s2 , 2p6 , 3s2 , 3p5
S16 : 1s2 , 2s2 , 2p6 , 3s2 , 3p4
جهد التأين الأول للكلور أكبر جهد التأين الاول للكبريت
- وذلك لأن في الدورات الأفقية في الجدول الدوري تزداد قيم جهد التأين الأولي كلما اتجهنا ناحية يمين الجدول أي بزيادة العدد الذرى.
والسبب في ذلك نقص نصف قطر الذرة (نقص الحجم) مما يؤدى إلى اقتراب إلكترونات التكافؤ من النواة فتحتاج إلى طاقة كبيرة لفصلها عن الذرة.
جهد التأين الثاني للكبريت أكبر من جهد التأين الثاني للكلور
- لأن عدد الألكترونات فى المستوى الخارجي فى الكبريت تناقص ( فى حالة جهد التأين الثاني وأصبحت (4) إلكترونات (نصف ممتلئ) وقريبة جداً من النواة على عكس الكلور الذى أصبح عدد الألكترونات فى المستوى الخارجي له (5) ولذلك يعنى جهد التأين الثاني للكبريت أعلى بقليل من جهد التأين الثاني للكلور وتحتاج طاقة أكبر لفصل هذا الألكترون الثاني فى الكبريت.