تعيين الصيغة الجزيئية لأى مركب
لتعيين وايجاد الصيغة الجزيئية للمادة نتبع الخطوات الآتية:-
(1) نستخرج الصيغة الوضعية للمادة كما فى هذا الموضوع: حساب الصيغة الوضعية.
(2) نحسب الكتلة المولية للصيغة الوضعية، وذلك من جمع الكتل الذرية لعناصرها.
(3) إيجاد الكتلة المولية للمادة (الصيغة الجزيئية)
(4) تقسيم الكتلة المولية للصيغة الجزيئية على الكتلة المولية للصيغة الوضعية لنحصل على وحدات الصيغة الوضعية.
وحدات الصيغة الوضعية يمكن الحصول عليها باستخدام العلاقة الاتية :
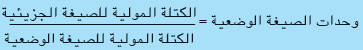
(5) ثم يضرب حاصل القسمة في الصيغة الوضعية للحصول على الصيغة الجزيئية.
حل المسألة
عينة من مركب نقي يحتوي على 43.7% فسفور و 56.3% أكسجين والكتلة المولية للمركب 284 جم/ مول . أوجد الصيغة الجزيئية؟
الحل:
أولاً: حساب الصيغة الأولية (الوضعية)
(1) نقسم كل نسبة مئوية للعنصر على كتلته الذرية أي أن:
نسبة عدد ذرات العنصر= النسبة المئوية للعنصر \ كتلته الذرية
أبسط نسبة لعدد ذرات الفوسفور= 43.7/31 = 1.41
ابسط نسبة لعدد ذرات الأكسجين = 56.3/16 = 3.52
(2) نقسم النسب السابقة على اصغرها نسبة ونقرب لاقرب عدد صحيح
أبسط نسبة لعدد ذرات العنصر = نسبة عدد ذرات كل عنصر \ أصغر نسبة
ابسط نسبة لعدد ذرات الفوسفور= 1.41/1.41 = 1
ابسط نسبة لعدد ذرات الأكسجين = 3.52/1.41= 2.5
وبالضرب في (2) نحصل على الصيغة الوضعية للمركب هي P2O5
ثانياً: حساب الصيغة الجزيئية
الكتلة المولية للصيغة الوضعية P2O5
= (2 × 31) + (5 × 16) = 142g/mol
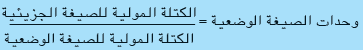
= 284/142 = 2
الصيغة الجزيئية = الصيغة الوضعية × وحدات الصيغة الوضعية
الصيغة الجزيئية = 2 × P4O10 = P2O5
الصيغة الجزيئية هي P4O10