إضافة الماء (الإماهة) Hydration للألكينات
- تضاف عناصر الماء إلى الرابطة المزدوجة في الألكينات بوجود كمية حفزية من حمض الكبريتيك المركز أو حمض الفوسفوريك لتعطي كحولات ثانوية أو ثلثية وتتبع الإضافة قاعدة ماركينوكوف.
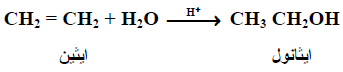
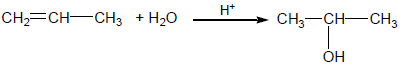
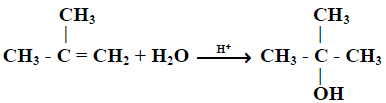
المسألة : إن إماهة كتلة 2.24 جم من ألكين (A) صيغته CnH2n أعطى كحول (B) كتلته 2.96 جم أعط الصيغة المجملة للكحول (B)؟
الحل:
معادلة التفاعل:
A + H2O → B
لاحظ ان (1) مول من الالكين يتفاعل مع (1) مول من الماء ليعطى (1) مول من الكحول
(1) حساب عدد المولات المتفاعلة من الألكين A
- الكتلة الجزيئية للألكين الذي صيغته CnH2n يساوي = 12n +1*2n = 14n
أى أن المول الواحد من الألكين (A) يساوي 14n جرام
- نفرض أن X هو عدد المولات المتفاعلة من الألكين فيكون:
1mole → 14n gm
X mole → 2.24 gm
بضرب الطرفين فى الوسطين نجد أن :
X = 2.24/14n
(2) حساب عدد المولات الناتجة من الكحول (B)
- الكتلة الجزيئية للكحول = الكتلة الجزيئية للألكين + الكتلة الجزيئية للماء وذلك لأن التفاعل هو تفاعل إضافة
- الكتلة الجزيئية للكحول = 14n + 18
أى أن المول الواحد من الكحول الناتج (B) يساوي (18 + 14n) جرام
- نفرض أن Y هو عدد المولات الناتجة من الكحول فيكون:
1mole → (14n + 18) gm
Y mole → 2.96 gm
بضرب الطرفين فى الوسطين نجد أن :
(18+Y = 2.96/(14n
- من معادلة التفاعل نجد أن 1 مول من الألكين (ِA) يعطى 1 مول من الكحول (B) أى أنه فى جميع الحالات:

- بوضع n = 4 تكون صيغة الألكين CnH2n هي C4H8 وتكون صيغة الكحول C4H8 + H2O أى تكون C4H10O
ملحوظة هامة : قد يكون للمسألة حل آخر أسهل ولكن هذا ما فكرت به.