حساب المولارية أو العيارية للأحماض والقواعد السائلة
- يتضمن الوعاء الذي يحتوي على المادة معلومات مثل النسبة المئوية للمادية % والكثافة (d) والوزن الجزيئي (M.wt)
ومن خلال هذة المعلومات يمكن حساب العيارية أو المولارية من القوانين الآتية:

سوف نقوم هنا بحساب مولارية المحلول الموجود فى الزجاجة.
- الوزن الجزيئي لحمض الهيدروكلوريك = 1 + 35.5 = 36.5 جم/مول
- النسبة المئوية الوزنية = 36.5%
- الكثافة = 1.05 جم /مول
وقم بالتعويض فى القانون أعلاه :
Molarity = 1.05 * 36.5 *10 / 36.5
10.5M =
مولارية حمض الهيدروكلوريك الموجود معنا هو 10.5M
والمطلوب تحضير 100 مل HCl تركيز 2M من المحلول HCl الذي تركيزه 10.5M لذلك نستخدم قانون التخفيف
قانون التخفيف
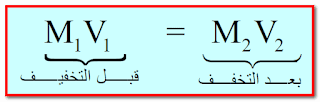
حيث :
M1 : تركيز المحلول الإبتدائي (قبل التخفيف)
M2 : تركيز المحلول النهائي (بعد التخفيف - أي عند إضافة مزيد من المذيب)
V1 : حجم المحلول الإبتدائي (قبل التخفيف - أي قبل إضافة المذيب)
V2 : حجم المحلول النهائي (بعد التخفيف - أي بعد إضافة المذيب)
من المعطيات السابقة
M1 = 10.5 , M2 = 2 , V1 = ?? ml , V2 =100ml
وبالتعويض فى القانون نجد أن :
M1 * V1 = M2 * V2
100 * 2 = V1 * 10.5
V1 = 19 ml
حجم الماء المضاف = حجم المحلول بعد التخفيف (V2) - حجم المحلول قبل التخفيف (V1)
حجم الماء المضاف = 100 - 19 = 81 مل
لتحضير 100 مل من HCl تركيزه 2M نضيف 19 مل من HCl الذي تركيزه 10.5M إلى 81 مل من الماء