قانون التخفيف Diluting law
- وفيه تتم إضافة المزيد من المذيب إلى محلول ذي تركيز معين.
- وبالتالي فإن تركيز المحلول يقل بسبب زيادة الحجم،إلا أن كمية المذاب تظل كما هي قبل وبعد التخفيف.
- وبالتالي فعدد المولات قبل التخفيف يساوي عدد المولات بعد التخفيف.
- ونعلم أن عدد المولات يحسب من حاصل ضرب التركيز بالمولارية (M) في حجم المحلول باللتر أو بالمللتر.
القانون :
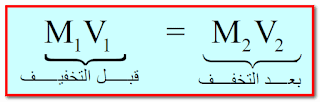
حيث :
M1 : تركيز المحلول الإبتدائي (قبل التخفيف)
M2 : تركيز المحلول النهائي (بعد التخفيف - أي عد إضافة مزيد من المذيب)
V1 : حجم المحلول الإبتدائي (قبل التخفيف - أي قبل إضافة المذيب)
V2 : حجم المحلول النهائي (بعد التخفيف - أي بعد إضافة المذيب)
حل المسألة
M1 = 0.2 , M2 = ?? , V1 =150ml
حجم المحلول بعد التخفيف (V2) = حجم المحلول قبل التخفيف (V1) + حجم الماء المضاف
V2 = 150 + 250 = 400ml
وبالتعويض فى القانون نجد أن :
M1 * V1 = M2 * V2
150 * 0.2 = 400 * M2
M2 = 0.075M